-
01
呼气检测

这是目前最常用的检测乳糖消化不良的方法,尽管在 4-5 岁以下儿童中使用时存在局限性。 患者口服一种含有乳糖的溶液(200-400 毫升水中含有 25-50 克乳糖),每隔 15 分钟,让他们向收集样本的密封袋/检测仪器/试管中呼气。 当未消化的糖被输送到大肠时,大肠中的细菌将其作为食物,并产生氢气作为废物。 氢被血液吸收并通过呼吸排出。 呼吸中检测到氢则表明糖已经进入大肠,没有在小肠中正常吸收。 摄入超过 20ppm 的乳糖后,呼吸中的氢必须增加,才表明存在消化不良。 为了避免可能的假阳性(尤其是在肠道菌群不产生氢气作为反应的人群中),还需要对甲烷的存在进行检测。在这种情况下,摄入乳糖后检测到的增加量必须高于 12ppm。 样本敏感度结果 (Isomed Pharma)
-
02
乳糖超荷/耐受性血液检测

这是另一种测量乳糖消化率的方法,但被认为不如前者可靠。 在这种方法中,首先从患者身上采集血液,以了解他们的基础血糖(血液中葡萄糖的初始或参考水平)。 然后,就像在氢检测中一样,让患者口服含 100 克乳糖的水溶液。 然后,在 60 分钟和 120 分钟后,采集新的血液样本。 如果没有葡萄糖的释放(由于缺少了肠道中本应存在的乳糖酶的作用),葡萄糖不会通过肠壁吸收到血液中,因此血液中的葡萄糖水平不会增加。 所以,不能说这是乳糖不耐受。 如果服用乳糖后血糖水平相对于基础(初始)值上升不超过 20 毫克/分升,则可以说存在乳糖消化不良。 患者敏感度的阳性和阴性结果示例。患者敏感度样本结果
-
03
小肠活检
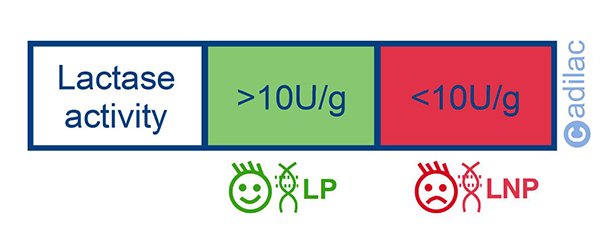
这是一种能够测量 LNP 的方法。 这是一种侵入性方法,因为获取样本进行后验分析是通过上消化道(十二指肠或空肠)的内窥镜检查或 EGD(食管胃十二指肠镜检查)进行的。 该检查通常在患者完全镇静的情况下进行。 通过鼻子或嘴向上消化道插入一根柔性光纤管(内窥镜检查)。 在内窥镜检查中获得的组织样本被送往实验室进行检查,并评估所提取的组织/粘膜的乳糖酶活性。 乳糖酶活性低于 10U/g 蛋白被认为与 LNP 或乳糖酶缺乏有关。
-
04
基因检测

原发性乳糖酶缺乏症 (LNP) 与遗传决定有关。 关于这方面,最新研究证实,乳糖酶活性与 MCM6 基因中发现的两个多态性有关。 该方法包括提取和扩增样本(患者的血液或唾液)的 DNA,继续进行条带杂交,以检测某些基因型的存在:携带 C/T 13910 多态性 CC 基因型和 G/A 22018 多态性 GG 基因型的个体存在原发性低乳糖酶症。 最后的实际结果是在一个条带上的一系列色带,这些色带在模板的帮助下进行解释。 研究结果为专家提供了乳糖酶缺乏症或 LNP 的遗传易感性信息。 敏感度结果示例 (Operon)
-
05
乳木糖检测

这种最新的方法能够对乳糖消化水平进行检测。 诊断是基于口服小剂量的乳木糖(化学名称 4-半乳糖木糖),一种类似乳糖的合成双糖,通过肠乳糖酶水解成半乳糖和木糖,后者通过尿液排出。 尿液中木糖的含量与肠道乳糖酶活性水平成正比,因此这个值可以用来检测乳糖消化不良的程度,并帮助诊断获得性或原发性低乳糖酶症。 如果前五小时内所有尿液中的木糖排泄量小于 19.18 毫克,则患者患有低乳糖酶症。 这是一种直接检测乳糖酶活性的方法,使用的糖剂量非常低,在检测过程中通常不会引起不适。 样品灵敏度结果 (Venter Pharma)
-
06
其他方法

粪检 pH 值测定:对于怀疑患乳糖不耐症的哺乳期婴儿,可通过直肠检查获得新鲜粪便样本,用最液态部分通过反应条进行 pH 值测定,从半点到半点进行区分检查酸度,并通过 Clinitest 片剂或 Clinitix 反应条测定还原剂和/或葡萄糖的存在。








